Донорство крови: проблема железодефицита у доноров

Переливание крови - важная, а порой единственная терапия, способная спасти жизнь людям, которые столкнулись с серьёзными травмами, ранениями, ожогами или хирургическими вмешательствами.
В мире
сдается:
>100 млн
единиц крови1
В РФ
общее число доноров ежегодно растет:
1,4 млн
составило в 2022 году человек2,
согласно данным
отчета Службы Крови.

Попытки лечения болезней чужой кровью известны еще из древних времен. Крови приписывали чудодейственные и омолаживающие свойства, рекомендовали пить кровь животных или здоровых людей при различной патологии.
Первые успешные попытки переливания крови от животного человеку были произведены в 1667 году во Франции, а от человека человеку – в 1882 году в Англии3.

По мере развития науки и медицины, открытия групп крови, законов изогемагглютинации и получения других новых знаний донорство крови как метод лечения получило широкое распространение и признание4.
В России отдельные попытки переливания крови известны с середины XIX века, а современная история донорства нашей стране берёт свое начало с 30-х годов XX столетия5.
На сегодняшний день человек является единственным источником крови для процедуры переливания, и заменить его кровь искусственной не представляется возможным. В связи с этим вопросы поддержки и сохранения здоровья доноров имеют первостепенное значение.
Общее влияние донорства на здоровье изучается примерно с 70 годов прошлого столетия. В исследованиях было показано, что дефицит железа чаще встречается у доноров крови, чем у людей, которые ими не являются6,7.
Долгое время также отсутствовали данные хорошо спланированных рандомизированных исследований о том, какие интервалы между донациями являются безопасными. Во многих странах стандартной практикой оставалось разрешение сдавать кровь с интервалом 8 недель. В 2019 году были опубликованы результаты исследования INTERVAL, в котором были проанализированы данные от 50 000 доноров, интервалы сдачи крови которых варьировались от 8 до 41 недели. В исследовании было показано, что частое донорство позволяло накопить большее количество крови и не оказывало существенного влияния на самочувствие, физическую активность и в целом на качество жизни доноров, что позволило службам по сбору крови рекомендовать продолжать использовать 8 и 12-недельные интервалы для донаций. Однако эти же интервалы были связаны со снижением гемоглобина и запасов железа, а также с симптомами железодефицитной анемии среди участников исследования9.
Таким образом, на сегодняшний день известно, что дефицит железа является негативным последствием донорства крови, вероятность развития которого во многом зависит от частоты донаций. В этическом аспекте врачи должны знать о том, как правильно диагностировать, профилактировать и вовремя восполнять запасы железа у тех, кто в этом нуждается.
Железо является важным микроэлементом в организме человека и имеет принципиальное значение для метаболизма, пролиферации и выживания клеток. Оно необходимо для транспорта кислорода, участвует в синтезе ДНК, дыхании и энергообмене клетки, синтезе коллагена и нейротрансмиттеров, а также в иммунном ответе на инфекции и процессах детоксикации10-13.
Дефицит железа приводит к:
Избыток железа имеет токсическое воздействие на организм: он генерирует активные формы кислорода, которые могут вызывать повреждение клеток и тканей14.
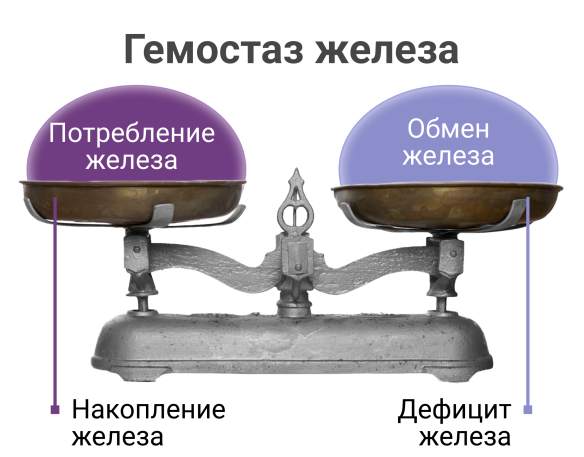
Таким образом, железо, в зависимости от его концентрации, может иметь как положительное, так и отрицательное действие на организм, что требует регуляции его клеточных уровней. Гомеостаз железа поддерживается за счёт уравновешивания поступления железа, его обмена и выведения15.
Ферритин является основным белком для хранения и переноса запасов железа. Он участвует в превращении двухвалентного железа (Fe 2+) в трехвалентное (Fe 3+), в виде которого железо поступает непосредственно в клетки16. С другой стороны, ферритин улавливает и буферизует избыток внутриклеточного железа, препятствуя его повреждающему воздействию17, то есть играет важную роль для поддержания его гомеостаза.
Про тест на ферретин| Показатели нормы | Показатели латентной стадии | Показатели ЖДА | |
| Ферритин (мкг/л) | 30-300 | <30 | <15 |
| Насыщение трансферрина (%) | 20-45 | <20 | <20 |
| Гемоглобин (г/дл) | Норма (12-13) | Норма (12-13) | Пониженный (<12-13) |
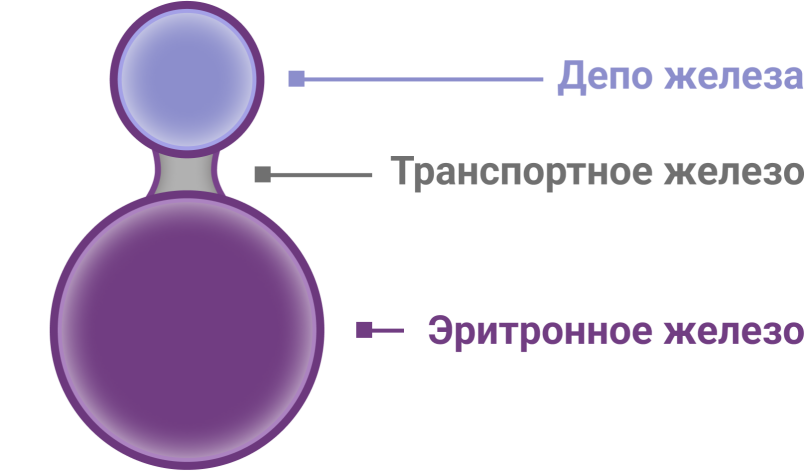

Нет изменений в клинических и лабораторных данных, есть усиленное всасывание железа в ЖКТ, которое можно определить только в условиях медицинского стационара

Характеризуется уменьшением запасов железа в организме по данным лабораторного обследования – снижение уровня ферритина ниже 30 мкг/л

Диагноз устанавливается при уровне гемоглобина менее 130 г/л у мужчин и 120 г/л у женщин.
Дополнительными параметрами ЖДА считают показатели ниже нормальных значений у: гематокрита, среднего объема эритроцитов, уровня ферритина, а также содержания сывороточного железа в сыворотке крови18.
Клиническими признаками латентного железодефицита являются:
Авторы крупномасштабных исследований в последние годы предлагают признать латентный дефицит железа (дефицит железа без анемии, Non-anemic iron deficiency) диагнозом, который требует быстрой диагностики и лечения21.
Основными признаками ЖДА являются все вышеперечисленные симптомы, характерные для латентного дефицита железа, а также:
ЖДА, определяемая на практике главным образом по уровню гемоглобина в клиническом анализе крови, является последней стадией дефицита железа. Становится очевидно, что одного измерения гемоглобина недостаточно для того, чтобы установить железодефицит у доноров крови22.Для диагностики абсолютного дефицита железа рекомендуется определять уровни ферритина, трансферрина, железа сыворотки крови, а также железосвязывающую способность сыворотки (ОЖСС) и коэффициент насыщения трансферрина железом (НТЖ)23.
Определение уровня ферритина, как предполагают ученые, является надёжным индикатором запасов железа в организме и позволяет определить его дефицит на ранней стадии24,25. Уровень ферритина в сыворотке <11 нг/мл отражает состояние истощения запасов железа. Пограничными считают уровни ферритина 30–50 нг/мл (или 30-50 мкг/л).

Целью лечения ЖДА и латентного дефицита железа является восполнение запасов железа в тканях и нормализация лабораторных показателей крови: уровень гемоглобина выше 120 г/л у женщин и 130г/л у мужчин, ферритин сыворотки крови выше 40–60 мкг/л. Как для лечения, так и для профилактики дефицита железа применяются пероральные и парентеральные препараты.

Рекомендуется также сочетать приём железа с поливитаминами (аскорбиновая кислота, фруктоза, цистеин) для улучшения процессов его усвоения23,26,27.


В исследованиях по изучению скорости восстановления показателей гемоглобина с применением различных препаратов двух- и трехвалентного железа Сорбифер Дурулес показал в 2 раза более высокий суточный прирост гемоглобина в сравнении с препаратами трёхвалентного железа29.
Свою эффективность по выраженному восстановлению уровня гемоглобина Сорбифер Дурулес также продемонстрировал у разных групп пациентов: беременных женщи30, в том числе с постковидной анемией31, пациентов, находящихся на гемодиализе32, женщин с обильными менструациями, а также заболеваниями желудочно-кишечного тракта (ЖКТ) и сердечно-сосудистой системы33.

Парентеральные препараты железа назначают в том случае, если лечение пероральными формами было не эффективно, а также при невозможности приёма препаратов через рот (наличие противопоказани23,26,27.
Длительность терапии определяется тяжестью исходного железодефицита, выбранным лечением, особенностями конкретного пациента и составляет в среднем от 1 до 3 месяцев26,27.

При применении препаратов железа возможны побочные эффекты в виде признаков раздражения желудка (тошнота, дискомфорт в эпигастральной области и т. д.), поэтому рекомендуется принимать таблетки во время еды.
Во время терапии препаратами железа обязательно проводится мониторинг показателей крови, а также самочувствия и состояния пациента23,26,27.
В первую очередь рекомендации по профилактике дефицита железа для доноров крови должны включать диспансерное наблюдение и регулярное обследование.
Стандартные показатели клинического анализа крови должны определяться перед каждой донацией, анализ крови на ферритин рекомендуется сдавать при частоте донаций более 1 в го8.
На сегодняшний день вопрос о профилактическом применении добавок железа донорами на постоянной основе остаётся дискуссионным. В 2017 году Ассоциация развития трансфузионной и биотерапии (AABB, Association for the Advancement of Blood and Biotherapies) опубликовала Бюллетень, в котором изложила рекомендации по профилактике железодефицита: создание и постоянное обновление учебных материалов для врачей и доноров, прием добавок железа на постоянной основе, регулярное определение уровня ферритина, увеличение интервалов между донациями34.
Помимо специальных рекомендаций доноры крови, так же, как и остальные люди, должны придерживаться принципов рационального питания с обеспечением поступления в организм достаточного количества железа с пищей.
Контент на данном сайте предназначен для работников здравоохранения. Нажимая на кнопку «Подтверждаю», вы подтверждаете, что являетесь работником здравоохранения РФ. Если вы не являетесь работником здравоохранения, то просьба покинуть данный сайт.